Soluciones simples y sostenibles que faciliten mejoras en la calidad de los datos sin impactar la innovación y la libertad investigadora.
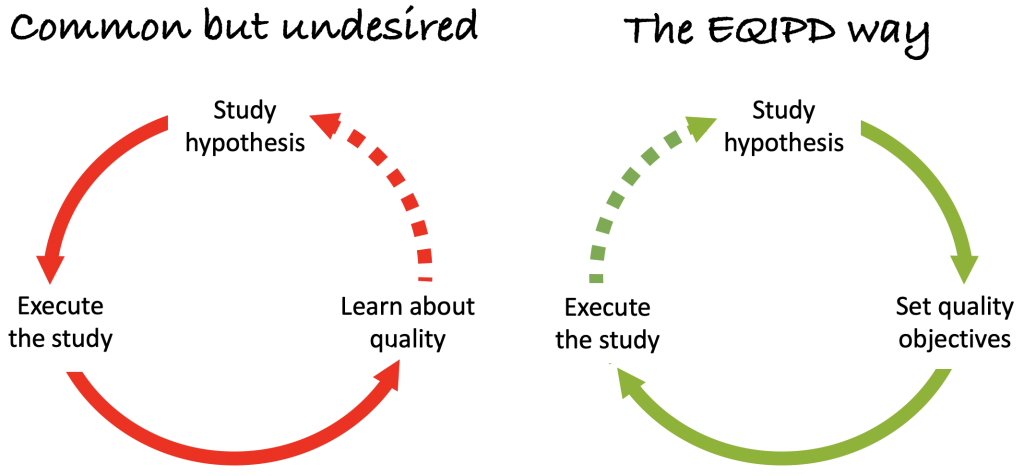
A menudo se habla sobre la calidad de los resultados científicos únicamente después de planear, ejecutar y finalizar los experimentos (diagrama de la izquierda), lo que resulta, en muchos casos, en una pérdida de tiempo y recursos.
El objetivo principal de EQIPD es asegurar que todos los requisitos críticos sobre la calidad investigadora se consideren e implementen durante la fase de diseño de los estudios y antes de que estos se lleven a cabo (esquema de la derecha).
Para lograr estos objetivos, EQIPD ha desarrollado:
- Un Sistema de Calidad, incluyendo apoyo para su implementación,
- un programa para apoyar a los equipos de investigación desde la preparación de una nueva propuesta de proyecto hasta la fase de ejecución,
- una serie de seminarios y talleres de formación para jóvenes científicos.
Póngase en contacto con el equipo de EQIPD con christoph.emmerich@paasp.net o renza.roncarati@paasp.net para obtener más información y asistencia en español, así como apoyo a proyectos en España y Latinoamérica.

Sobre EQIPD
El consorcio Enhancing Quality in Preclinical Data (EQIPD) ha desarrollado herramientas simples y sostenibles para garantizar datos de calidad sin afectar la innovación y la libertad de investigación.
El consorcio EQIPD, fundado en 2017, trabaja en estrecha colaboración con instituciones de investigación, editoriales, financiadores, sociedades científicas y sociedades profesionales de casi 110 organizaciones en Europa y Estados Unidos.
Este sitio web ha sido creado y es mantenido por el grupo de trabajo de EQIPD, responsable del mantenimiento a largo plazo y la difusión del Sistema de Calidad de EQIPD y los recursos y servicios asociados.
Visite el sitio web para obtener información sobre otras iniciativas del consorcio EQIPD.

¿Cuáles son las ventajas de obtener la etiqueta de calidad EQIPD?
Al tratarse de una evaluación independiente de su programa de investigación, ayuda a su unidad a establecer un diseño experimental mejorado y producir datos más sólidos.
Aumenta la confianza en los datos entregados por un colaborador, un socio de investigación, un proveedor de servicios o un beneficiario.
Facilita la toma de decisiones en un programa de investigación o en la selección de socios de investigación o proveedores de servicios (mitigación de riesgos).
El sistema de calidad EQIPD
Con el apoyo de la Iniciativa de Medicamentos Innovadores (Innovative Medicines Initiative, IMI) de la Unión Europea, EQIPD ha desarrollado un novedoso sistema de calidad para la investigación preclínica que puede aplicarse tanto en el sector público como en el privado. Nuestro Sistema de Calidad asegura la generación de datos preclínicos robustos y de confianza a la vez que es ágil y efectivo, impulsando así la innovación. Sirve a las necesidades de la investigación biomédica no regulada (es decir, áreas en las que los sistemas formales de gestión de la calidad como las Buenas Prácticas de Laboratorio [BPL, GLP] no se consideran apropiados).
El sistema de calidad EQIPD proporciona un marco estable para el mantenimiento a largo plazo de altos estándares de investigación. No es solo una colección de pautas e instrucciones, sino más bien es:
- Una herramienta para coordinar y dirigir las actividades de una organización para cumplir con los objetivos de calidad y mejorar la efectividad y eficiencia de la organización de manera continua;
- un “espejo” que los investigadores pueden utilizar para evaluar cómo realizan sus experimentos y qué es necesario cambiar o mejorar.
Para obtener más información, visite la plataforma wiki del Sistema de Calidad EQIPD, un esfuerzo colaborativo de la comunidad EQIPD para crear y compartir información sobre las mejores prácticas, herramientas y recursos de investigación.

El Sello de Calidad EQIPD
EQIPD ofrece a las unidades de investigación (laboratorios, departamentos, empresas, etc.) dos opciones diferentes para obtener un Sello de Calidad.
Opción 1 (Certificación del Sistema de Calidad)
la implementación del Sistema de Calidad EQIPD por parte del cuerpo de investigación interesado es evaluada por el equipo de EQIPD, y resultados satisfactorios resultan en una certificación completa durante 3 años.
Opción 2 (Certificación específica)
una solución flexible impulsada por las necesidades de un proyecto de colaboración específico. El equipo de EQIPD evalúa las prácticas de calidad actuales para el cumplimiento de las expectativas de EQIPD. El certificado, más limitado, es válido por un período de hasta 1 año.

Apoyo a proyectos
EQIPD brinda apoyo a organizaciones que están desarrollando nuevos proyectos o solicitudes de subvenciones y están interesadas en introducir capacitación, evaluaciones y monitoreo de calidad de investigación adicionales, por ejemplo, en forma de paquete de trabajo independiente dentro de las propuestas de proyectos.
Este soporte se divide en tres partes:
- Parte 1 – Formación general sobre buenas prácticas de investigación;
- Parte 2 – Evaluaciones iniciales de las prácticas de calidad, planificación rigurosa de la investigación e implementación de soluciones prácticas para la mejora (si fuera necesario);
- Parte 3 – Controles al azar para probar el cumplimiento del plan de estudio predefinido y las buenas prácticas de investigación, así como la evaluación de la gestión de errores y accidentes críticos.

Formación
EQIPD ofrece programas de capacitación en varios formatos que van desde breves conferencias introductorias (2-4 horas) hasta cursos de capacitación y series de seminarios para estudiantes, investigadores post-doctorales, investigadores jóvenes y científicos establecidos.
El programa de formación EQIPD cubre aspectos clave de la calidad de los datos en la investigación biomédica, incluyendo:
- Discusión sobre “reproducibilidad”: alcance del problema
- Robustez vs reproducibilidad
- Orígenes de la escasa solidez en los datos
- Estudio de diseño y poder estadístico
- Valor predictivo positivo
- Importancia del control sobre las condiciones experimentales
- Generalizabilidad de los resultados de la investigación
- Elementos clave de las buenas prácticas de investigación
- Presentación de detalles metodológicos
- Aplicación de estándares de diseño de estudios clínicos en investigación preclínica
- Confirmación de los resultados de la investigación en una gama más amplia de condiciones
- Presentación correcta del análisis de datos estadísticos
- Cultura de tolerancia a datos negativos
- Consecuencias de la falta de rigor científico.

